[Fuvest 2021] O gás carbônico atmosférico reage com a água do mar conforme detalhado em (I):
(I) ![]()
As condições ambientais causadas pelo aumento do gás carbônico na atmosfera influenciam em processos caracterizados pela reação (II) durante o desenvolvimento de diversos organismos marinhos:
(II) ![]()
Tendo por base essas afirmações, assinale a alternativa correta:
Note e adote:
Considere o bicabornato solúvel e o carbonato de cálcio insolúvel
- O processo (I) resulta em diminuição da alcalinidade da água do mar, comprometendo a estruturação de recifes por interferir na formação dos esqueletos calcários dos corais, conforme a reação (II).
- O processo (I) resulta em aumento da alcalinidade da água do mar, comprometendo processos de contração muscular de vertebrados marinhos por diminuir o cálcio livre disponível, como demonstrado em (II).
- O processo (I) não altera a alcalinidade da água do mar, mas compromete o processo de formação de conchas de moluscos marinhos, nos quais a estrutura básica é o carbonato de cálcio, produto da reação (II).
- O processo (I) resulta em diminuição da alcalinidade da água do mar, aumentando o pH e beneficiando o processo demonstrado em (II), o que favorece o crescimento de recifes de algas calcárias.
- O processo (I) resulta em aumento da alcalinidade da água do mar, beneficiando os processos de fermentação por bactérias marinhas em regiões de recifes de coral, que são formados pelo processo (II).
[Fuvest 2021] O diagrama ao lado representa algumas espécies que podem ser formadas quando o Fe metálico é exposto a diferentes condições de pH e potencial de redução medidos contra o eletrodo padrão de hidrogênio. As regiões relativas às espécies ![]() e
e ![]() estão associadas às regiões marcadas como (I) e (II) no diagrama, não necessariamente nessa ordem.
estão associadas às regiões marcadas como (I) e (II) no diagrama, não necessariamente nessa ordem.
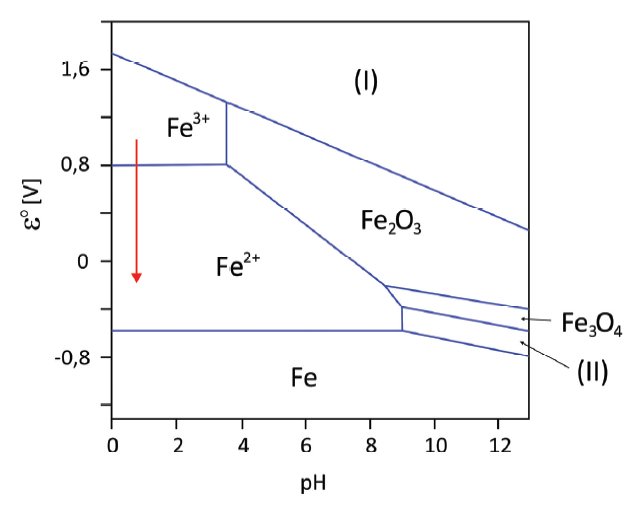
a) Para evitar a corrosão de um objeto de ferro metálico, este foi submetido a pH e potencial adequados, formando uma camada de ![]() na superfície. Explique como essa camada previne a corrosão do interior do objeto.
na superfície. Explique como essa camada previne a corrosão do interior do objeto.
b) Escreva a semirreação de redução associada ao processo representado pela seta, indicando o valor de potencial a partir do qual a reação acontece.
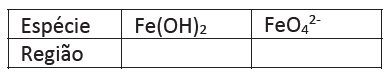
c) Associe, corretamente, na tabela da folha de resposta, cada uma das regiões (I) e (II) com as espécies ![]() e
e ![]() . Justifique a associação feita com base nos potenciais de redução apresentados no diagrama.
. Justifique a associação feita com base nos potenciais de redução apresentados no diagrama.
[Unicamp 2021] A remoção de sulfeto de hidrogênio presente em amostras de biogás é essencial, já que ele é altamente corrosivo para tubulações metálicas. A queima desse ![]() também é muito prejudicial ao meio ambiente, pois leva à formação de dióxido de enxofre. Um estudo de 2014 sugere que a remoção do
também é muito prejudicial ao meio ambiente, pois leva à formação de dióxido de enxofre. Um estudo de 2014 sugere que a remoção do ![]() pode ser realizada pelo uso de esponjas de óxido de ferro, que reage com esse gás, mas pode ser regenerado. Segundo o estudo, no dispositivo utilizado, 1,00 kg de óxido de ferro foi capaz de remover entre 0,200 e 0,716 kg de sulfeto de hidrogênio. Considere que apenas a reação abaixo equacionada esteja ocorrendo nessa remoção.
pode ser realizada pelo uso de esponjas de óxido de ferro, que reage com esse gás, mas pode ser regenerado. Segundo o estudo, no dispositivo utilizado, 1,00 kg de óxido de ferro foi capaz de remover entre 0,200 e 0,716 kg de sulfeto de hidrogênio. Considere que apenas a reação abaixo equacionada esteja ocorrendo nessa remoção.
![]()
A partir desses dados, pode-se afirmar que, na condição de remoção máxima de sulfeto de hidrogênio relatada no estudo,
Massas molares ![]() : Fe = 56, H = 1, O = 16 e S = 32.
: Fe = 56, H = 1, O = 16 e S = 32.
- restaram cerca de 33% de óxido de ferro para reagir, tomando por base a estequiometria da equação química fornecida.
- restaram cerca de 67% de óxido de ferro para reagir, tomando por base a estequiometria da equação química fornecida.
- foi removida uma quantidade maior de H2S que a prevista pela estequiometria da equação química fornecida.
- as quantidades reagiram na proporção estequiométrica da equação química fornecida.
[Fuvest 2020] O lítio foi identificado no século XIX a partir das observações do naturalista e estadista brasileiro José Bonifácio de Andrada e Silva. Em 2019, esse elemento ganhou destaque devido ao Prêmio Nobel de Química, entregue aos pesquisadores John Goodenough, Stanley Whittingham e Akira Yoshino pelas pesquisas que resultaram na bateria recarregável de íon lítio. Durante o desenvolvimento dessa bateria, foi utilizado um eletrodo de ![]() (semirreação I) em conjunto com um eletrodo de lítio metálico intercalado em grafita
(semirreação I) em conjunto com um eletrodo de lítio metálico intercalado em grafita ![]() (semirreação II) ou um eletrodo de lítio metálico
(semirreação II) ou um eletrodo de lítio metálico ![]() (semirreação III).
(semirreação III).

Considerando essas semirreações:
a) Escreva a reação global da bateria que utiliza o lítio metálico como um dos eletrodos.
b) Indique qual dos dois materiais, lítio metálico ou lítio metálico intercalado em grafita, será um agente redutor mais forte. Justifique com os valores de potencial de redução padrão.
Em 1800, José Bonifácio descobriu o mineral petalita, de fórmula ![]() (na qual X é um metal alcalino). Em 1817, ao assumir que X = Na, o químico sueco Johan Arfwedson observou que a petalita apresentaria uma porcentagem de metal alcalino superior ao determinado experimentalmente. Ao não encontrar outros substitutos conhecidos que explicassem essa incongruência, ele percebeu que estava diante de um novo elemento químico, o Lítio
(na qual X é um metal alcalino). Em 1817, ao assumir que X = Na, o químico sueco Johan Arfwedson observou que a petalita apresentaria uma porcentagem de metal alcalino superior ao determinado experimentalmente. Ao não encontrar outros substitutos conhecidos que explicassem essa incongruência, ele percebeu que estava diante de um novo elemento químico, o Lítio ![]() .
.
c) Explique, mostrando os cálculos, como a observação feita por Arfwedson permitiu descobrir que o elemento novo era o Lítio.
Note e adote:
Massas molares ![]() ;
; ![]() ;
; ![]() ;
; ![]() ;
; ![]() .
.
% em massa de ![]() na petalita: 8,8%.
na petalita: 8,8%.
[Fuvest 2020] O experimento conhecido como “chuva de ouro” consiste na recristalização, à temperatura ambiente, de iodeto de chumbo ![]() . A formação desse sal pode ocorrer a partir da mistura entre nitrato de chumbo
. A formação desse sal pode ocorrer a partir da mistura entre nitrato de chumbo ![]() e iodeto de potássio
e iodeto de potássio ![]() . Outro produto dessa reação é o nitrato de potássio
. Outro produto dessa reação é o nitrato de potássio ![]() em solução aquosa. Tanto o
em solução aquosa. Tanto o ![]() quanto o
quanto o ![]() são sais brancos solúveis em água à temperatura ambiente, enquanto o
são sais brancos solúveis em água à temperatura ambiente, enquanto o ![]() é um sal amarelo intenso e pouco solúvel nessa temperatura, precipitando como uma chuva dourada.
é um sal amarelo intenso e pouco solúvel nessa temperatura, precipitando como uma chuva dourada.
Em um laboratório, o mesmo experimento foi realizado em dois frascos. Em ambos, 100 mL de solução ![]() de
de ![]() e 100 mL de solução
e 100 mL de solução ![]() de
de ![]() foram misturados. Ao primeiro frasco foi também adicionado 20 mL de água destilada, enquanto ao segundo frasco foi adicionado 20 mL de solução
foram misturados. Ao primeiro frasco foi também adicionado 20 mL de água destilada, enquanto ao segundo frasco foi adicionado 20 mL de solução ![]() de iodeto de sódio
de iodeto de sódio ![]() .
.
A tabela a seguir apresenta os dados de solubilidade dos produtos da reação em diferentes temperaturas.

Responda aos itens a seguir considerando os dados do enunciado e o equilíbrio químico de solubilidade do iodeto de chumbo:
![]()
a) Indique se o procedimento do segundo frasco favorece ou inibe a formação de mais sólido amarelo.
b) Para separar o precipitado da solução do primeiro frasco e obter o ![]() sólido e seco, foi recomendado que, após a precipitação, fosse realizada uma filtração em funil com papel de filtro, seguida de lavagem do precipitado com água para se retirar o
sólido e seco, foi recomendado que, após a precipitação, fosse realizada uma filtração em funil com papel de filtro, seguida de lavagem do precipitado com água para se retirar o ![]() formado e, na sequência, esse precipitado fosse colocado para secar. Nesse caso, para se obter a maior quantidade do
formado e, na sequência, esse precipitado fosse colocado para secar. Nesse caso, para se obter a maior quantidade do ![]() , é mais recomendado o uso de água fria (4 °C) ou quente (80 °C)? Justifique.
, é mais recomendado o uso de água fria (4 °C) ou quente (80 °C)? Justifique.
c) Encontre a constante do produto de solubilidade ![]() do iodeto de chumbo a 32 °C.
do iodeto de chumbo a 32 °C.
1 2 Próximo › Último »