[Unifesp 2021] sequência de reações representada no esquema resume etapas de um dos processos de obtenção de ácido L-ascórbico (vitamina C) a partir da glicose.
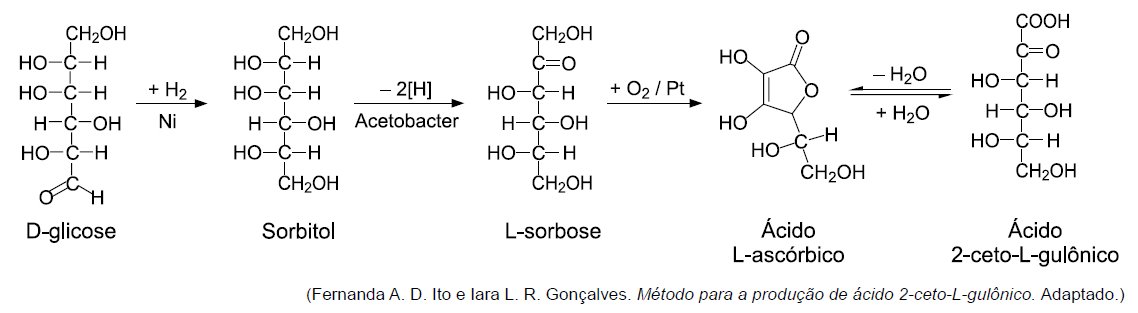
a) Dê o nome da substância que possui um grupo funcional éster. Quais substâncias, entre as representadas no esquema, são isômeras entre si?
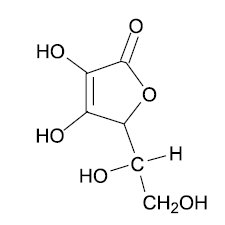
b) Dê o nome do composto que sofre redução na sequência de reações. Indique, na fórmula do ácido L-ascórbico presente no campo de Resolução e Resposta, os dois átomos de carbono assimétrico.
[Fuvest 2021] Os polímeros superabsorventes são compostos com alta capacidade de absorver água. Um desses polímeros é o poliacrilato de sódio (NaPA), mostrado na figura. O NaPA é formado a partir da polimerização de seu precursor, um ácido orgânico, seguida da neutralização dos grupos ácidos com hidróxido de sódio.

a) Desenhe, na folha de resposta, o monômero precursor do poliacrilato de sódio, na forma ácida.
O gráfico ao lado mostra a capacidade de absorção de água pelo NaPA para diferentes quantidades de sal (0; 1,0; 2,5; e 5,0%). No caso desse experimento, foi usado o cloreto de sódio, mas o mesmo resultado é observado para outros sais.
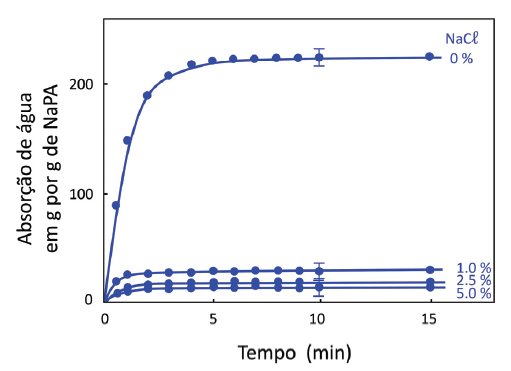
b) O NaPA é bastante utilizado como absorvedor em fraldas descartáveis. Nesse caso, a absorção da urina pela fralda será mais ou menos eficiente do que a da água destilada? Explique.
c) Indique qual o tipo de interação mais forte que ocorre entre a água e o polímero e explique o efeito da quantidade de sal na absorção de água, representado no gráfico.
[Unifesp 2020] Considere o experimento:
Uma porção de iodeto de sódio sólido, radioativo, cujo ânion ![]() – é radioativo, foi adicionada a uma solução aquosa saturada, sem corpo de fundo, de iodeto de sódio (
– é radioativo, foi adicionada a uma solução aquosa saturada, sem corpo de fundo, de iodeto de sódio (![]() ) não radioativo, formando uma solução saturada com corpo de fundo. Após algum tempo, a mistura foi filtrada e a intensidade da radiação foi verificada no sólido retido no filtro e na solução saturada. Foi constatado que a solução saturada, inicialmente não radioativa, tornou-se radioativa, e que o sólido apresentou menor intensidade de radiação do que apresentava antes de ser adicionado à solução.
) não radioativo, formando uma solução saturada com corpo de fundo. Após algum tempo, a mistura foi filtrada e a intensidade da radiação foi verificada no sólido retido no filtro e na solução saturada. Foi constatado que a solução saturada, inicialmente não radioativa, tornou-se radioativa, e que o sólido apresentou menor intensidade de radiação do que apresentava antes de ser adicionado à solução.
a) Calcule o número de nêutrons e de elétrons do ânion ![]() .
.
b) Escreva a equação química que representa o equilíbrio de solubilidade do iodeto de sódio em água. Baseando-se no conceito de equilíbrio químico e no comportamento das espécies químicas em nível microscópico, justifique por que a radioatividade do sólido diminuiu e a solução saturada tornou-se radioativa.
[Fuvest 2020] As concentrações de alguns íons em amostras de água estão representadas nos gráficos a seguir. A origem de cada amostra (1, 2 e 3) foi omitida, mas pode corresponder a: amostra de água do mar; amostra de água de chuva numa região costeira; amostra de água doce de rio.

a) O bicarbonato na água pode vir de diferentes fontes. Cite uma fonte de bicarbonato comum às três amostras.
b) Preencha a tabela da folha de respostas com a correspondência entre as amostras 1, 2 e 3 e o ambiente em que foram coletadas.
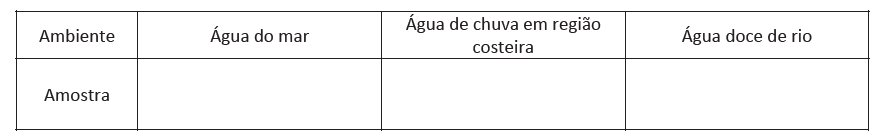
c) É esperado que a concentração de íons cloreto na água coletada da chuva em um ambiente continental seja igual, maior ou menor à de ambientes costeiros (ambos sem poluição)? Justifique sua resposta.
[Fuvest 2020] Arla 32 é uma solução de aproximadamente 32 g de ureia ![]() em 100 mL de água utilizada em veículos a diesel para diminuir as emissões de óxidos de nitrogênio (
em 100 mL de água utilizada em veículos a diesel para diminuir as emissões de óxidos de nitrogênio (![]() e
e ![]() ), que podem causar problemas ambientais quando em excesso na atmosfera. A solução de Arla, ao ser adicionada aos gases de escape do motor, em alta temperatura, forma amônia (reação I). Em uma segunda etapa, a amônia formada reage com
), que podem causar problemas ambientais quando em excesso na atmosfera. A solução de Arla, ao ser adicionada aos gases de escape do motor, em alta temperatura, forma amônia (reação I). Em uma segunda etapa, a amônia formada reage com ![]() e gera gás nitrogênio e água (reação II).
e gera gás nitrogênio e água (reação II).
(I) ![]()
(II) ![]()
a) Escreva a fórmula de Lewis da ureia.
b) Calcule quantos litros de solução de Arla 32 são necessários para consumir todo o ![]() produzido em uma viagem de 100 km, considerando que a quantidade de
produzido em uma viagem de 100 km, considerando que a quantidade de ![]() formado por esse veículo é de 460 mg por km rodado. Indique os cálculos.
formado por esse veículo é de 460 mg por km rodado. Indique os cálculos.
c) Considerando que a reação entre ![]() e
e ![]() forma os mesmos produtos que a reação II, o volume gasto de Arla 32 para consumir o
forma os mesmos produtos que a reação II, o volume gasto de Arla 32 para consumir o ![]() seria menor, igual ou maior ao usado para consumir uma mesma quantidade em mol de
seria menor, igual ou maior ao usado para consumir uma mesma quantidade em mol de ![]() ? Justifique mostrando a reação entre
? Justifique mostrando a reação entre ![]() e
e ![]() .
.
Note e adote:
Considerar todas as reações com 100% de rendimento.
Massas molares: ![]() ;
; ![]()
Distribuição eletrônica: ![]() ;
; ![]() ;
; ![]() ;
; ![]()
« Primeiro ‹ Anterior 1 2 3 4 5 6 8 Próximo › Último »