[Unifesp 2020] Os gases medicinais são utilizados em hospitais, clínicas de saúde ou outros locais de interesse à saúde, bem como em tratamentos domiciliares de pacientes. Considere a composição de quatro gases medicinais, acondicionados separadamente em quatro cilindros, I, II, III e IV, nas condições indicadas na tabela.
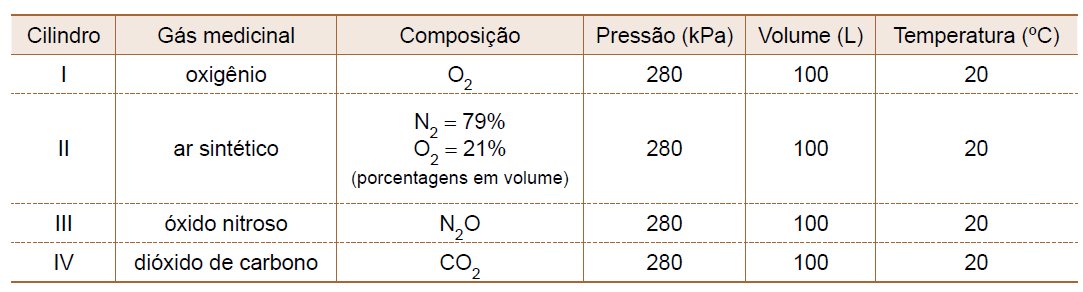
a) Identifique, entre os gases medicinais citados, aquele que é constituído por uma substância química simples e aquele que gera uma solução aquosa ácida ao ser borbulhado em água destilada.
b) Baseando-se no princípio de Avogadro, determine as seguintes proporções:
• número de moléculas no cilindro I : número de moléculas no cilindro II : número de moléculas no cilindro III : número de moléculas no cilindro IV.
• número de átomos de oxigênio no cilindro II : número de átomos de oxigênio no cilindro III.
[Unifesp 2020] O leite de magnésia é uma suspensão aquosa. Determinada embalagem desse produto mostra a seguinte composição:
Cada 15 mL contém: hidróxido de magnésio (1 282,50 mg), hipoclorito de sódio e água purificada.
Um grupo de estudantes resolveu utilizar uma amostra desse leite de magnésia, que se encontrava com data de validade expirada para ingestão humana, a fim de obter sulfato de magnésio hepta-hidratado, a ser utilizado em laboratório escolar como reagente para testes qualitativos. Para tanto, executaram o procedimento ilustrado a seguir.
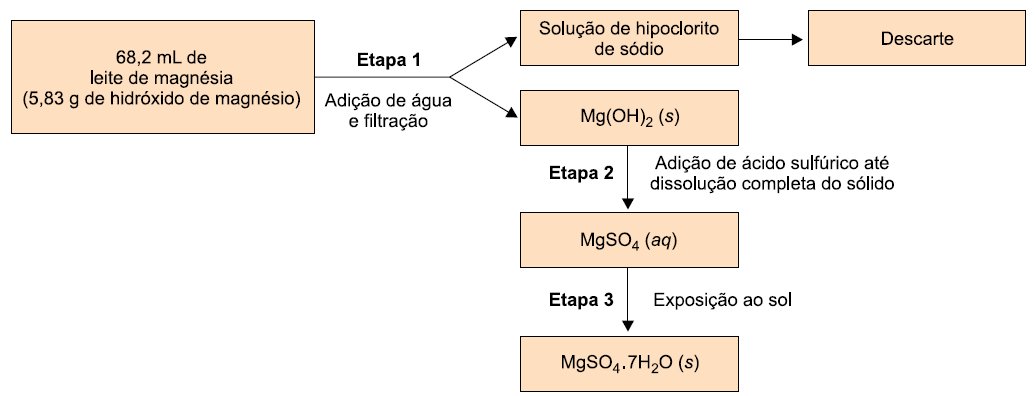
a) Represente, por meio de fórmula, as ligações químicas presentes no hidróxido de magnésio, ![]() . Cite o nome do método de separação de misturas empregado pelos estudantes na última etapa do procedimento.
. Cite o nome do método de separação de misturas empregado pelos estudantes na última etapa do procedimento.
b) Escreva a equação da reação química que ocorre na etapa 2. Calcule a massa de sulfato de magnésio hepta-hidratado obtida pelos estudantes, admitindo que o rendimento foi de 100%.
[Fuvest 2020] O lítio foi identificado no século XIX a partir das observações do naturalista e estadista brasileiro José Bonifácio de Andrada e Silva. Em 2019, esse elemento ganhou destaque devido ao Prêmio Nobel de Química, entregue aos pesquisadores John Goodenough, Stanley Whittingham e Akira Yoshino pelas pesquisas que resultaram na bateria recarregável de íon lítio. Durante o desenvolvimento dessa bateria, foi utilizado um eletrodo de ![]() (semirreação I) em conjunto com um eletrodo de lítio metálico intercalado em grafita
(semirreação I) em conjunto com um eletrodo de lítio metálico intercalado em grafita ![]() (semirreação II) ou um eletrodo de lítio metálico
(semirreação II) ou um eletrodo de lítio metálico ![]() (semirreação III).
(semirreação III).

Considerando essas semirreações:
a) Escreva a reação global da bateria que utiliza o lítio metálico como um dos eletrodos.
b) Indique qual dos dois materiais, lítio metálico ou lítio metálico intercalado em grafita, será um agente redutor mais forte. Justifique com os valores de potencial de redução padrão.
Em 1800, José Bonifácio descobriu o mineral petalita, de fórmula ![]() (na qual X é um metal alcalino). Em 1817, ao assumir que X = Na, o químico sueco Johan Arfwedson observou que a petalita apresentaria uma porcentagem de metal alcalino superior ao determinado experimentalmente. Ao não encontrar outros substitutos conhecidos que explicassem essa incongruência, ele percebeu que estava diante de um novo elemento químico, o Lítio
(na qual X é um metal alcalino). Em 1817, ao assumir que X = Na, o químico sueco Johan Arfwedson observou que a petalita apresentaria uma porcentagem de metal alcalino superior ao determinado experimentalmente. Ao não encontrar outros substitutos conhecidos que explicassem essa incongruência, ele percebeu que estava diante de um novo elemento químico, o Lítio ![]() .
.
c) Explique, mostrando os cálculos, como a observação feita por Arfwedson permitiu descobrir que o elemento novo era o Lítio.
Note e adote:
Massas molares ![]() ;
; ![]() ;
; ![]() ;
; ![]() ;
; ![]() .
.
% em massa de ![]() na petalita: 8,8%.
na petalita: 8,8%.
[Fuvest 2020] O experimento conhecido como “chuva de ouro” consiste na recristalização, à temperatura ambiente, de iodeto de chumbo ![]() . A formação desse sal pode ocorrer a partir da mistura entre nitrato de chumbo
. A formação desse sal pode ocorrer a partir da mistura entre nitrato de chumbo ![]() e iodeto de potássio
e iodeto de potássio ![]() . Outro produto dessa reação é o nitrato de potássio
. Outro produto dessa reação é o nitrato de potássio ![]() em solução aquosa. Tanto o
em solução aquosa. Tanto o ![]() quanto o
quanto o ![]() são sais brancos solúveis em água à temperatura ambiente, enquanto o
são sais brancos solúveis em água à temperatura ambiente, enquanto o ![]() é um sal amarelo intenso e pouco solúvel nessa temperatura, precipitando como uma chuva dourada.
é um sal amarelo intenso e pouco solúvel nessa temperatura, precipitando como uma chuva dourada.
Em um laboratório, o mesmo experimento foi realizado em dois frascos. Em ambos, 100 mL de solução ![]() de
de ![]() e 100 mL de solução
e 100 mL de solução ![]() de
de ![]() foram misturados. Ao primeiro frasco foi também adicionado 20 mL de água destilada, enquanto ao segundo frasco foi adicionado 20 mL de solução
foram misturados. Ao primeiro frasco foi também adicionado 20 mL de água destilada, enquanto ao segundo frasco foi adicionado 20 mL de solução ![]() de iodeto de sódio
de iodeto de sódio ![]() .
.
A tabela a seguir apresenta os dados de solubilidade dos produtos da reação em diferentes temperaturas.

Responda aos itens a seguir considerando os dados do enunciado e o equilíbrio químico de solubilidade do iodeto de chumbo:
![]()
a) Indique se o procedimento do segundo frasco favorece ou inibe a formação de mais sólido amarelo.
b) Para separar o precipitado da solução do primeiro frasco e obter o ![]() sólido e seco, foi recomendado que, após a precipitação, fosse realizada uma filtração em funil com papel de filtro, seguida de lavagem do precipitado com água para se retirar o
sólido e seco, foi recomendado que, após a precipitação, fosse realizada uma filtração em funil com papel de filtro, seguida de lavagem do precipitado com água para se retirar o ![]() formado e, na sequência, esse precipitado fosse colocado para secar. Nesse caso, para se obter a maior quantidade do
formado e, na sequência, esse precipitado fosse colocado para secar. Nesse caso, para se obter a maior quantidade do ![]() , é mais recomendado o uso de água fria (4 °C) ou quente (80 °C)? Justifique.
, é mais recomendado o uso de água fria (4 °C) ou quente (80 °C)? Justifique.
c) Encontre a constante do produto de solubilidade ![]() do iodeto de chumbo a 32 °C.
do iodeto de chumbo a 32 °C.
[Fuvest 2020] Muitos metais ![]() em água, dependendo do pH da solução, formam hidróxidos
em água, dependendo do pH da solução, formam hidróxidos ![]() insolúveis.
insolúveis.
Esse comportamento pode ser descrito pela equação (I), que relaciona o valor de pH com o logaritmo da concentração do metal ![]() , para uma dada temperatura, em que
, para uma dada temperatura, em que ![]() é a constante do produto de solubilidade do hidróxido do metal.
é a constante do produto de solubilidade do hidróxido do metal.
Equação (I): ![]()
O comportamento da equação (I) é representado no gráfico, no qual as linhas mostram o valor de pH e ![]() em que se inicia a precipitação de cada um dos metais. Em condições mais alcalinas do que a apresentada na linha de cada metal, será observada a espécie insolúvel como hidróxido e, em condições mais ácidas do que a apresentada na linha, será observada a espécie em sua forma solúvel.
em que se inicia a precipitação de cada um dos metais. Em condições mais alcalinas do que a apresentada na linha de cada metal, será observada a espécie insolúvel como hidróxido e, em condições mais ácidas do que a apresentada na linha, será observada a espécie em sua forma solúvel.
a) Pinte, no gráfico da folha de respostas, a região onde o ![]() se encontra na forma solúvel e o
se encontra na forma solúvel e o ![]() se encontra na forma de
se encontra na forma de ![]() insolúvel.
insolúvel.
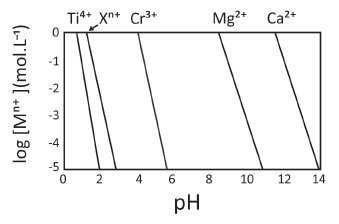
b) As linhas que representam ![]() e
e ![]() possuem a mesma inclinação, mas diferem da inclinação das linhas que representam
possuem a mesma inclinação, mas diferem da inclinação das linhas que representam ![]() e
e ![]() , que possuem a mesma inclinação entre si. Indique a carga n de
, que possuem a mesma inclinação entre si. Indique a carga n de ![]() e justifique com base na equação (I).
e justifique com base na equação (I).
c) Indique qual das espécies tem maior valor de ![]() :
: ![]() ou
ou ![]() . Justifique com base nas informações dadas.
. Justifique com base nas informações dadas.
« Primeiro ‹ Anterior 1 3 4 5 6 7 8 Próximo › Último »